br
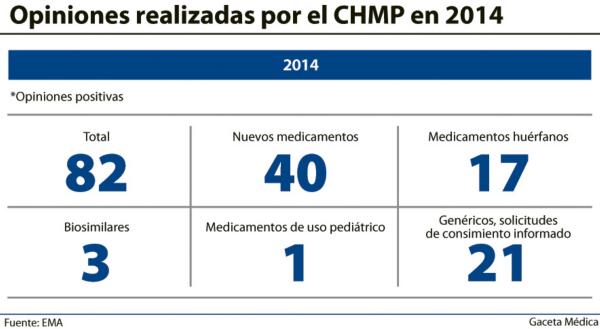
La Agencia Europea de Medicamentos (EMA) aprobó en 2014 un total de 82 nuevos medicamentos: 22 génericos/híbridos, tres biosimilares, 40 no huérfanos y 17 medicamentos huérfanos, de los cuales tres fueron recomendados por el Comité de Medicamentos de Uso Humano (CHMP), aunque sus solicitudes fueron retiradas por el promotor antes de la decisión final de la agencia.
En esta ocasión, la EMA vuelve a batir su propio record en medicamentos huérfanos. En 2011, aprobó cuatro fármacos; en 2012, ocho y tres más en 2013. No ocurrió lo mismo, respecto a los nuevos medicamentos, donde la cifra pasó de los 46 aprobados en 2013, a los 40 del año siguiente, y a los biosimilares que pasaron de cuatro a tres.
De entre los fármacos huérfanos aprobados, destaca atalurén —comercializado como Translarna por PTC Therapeutics— el primer medicamento para el tratamiento de la distrofia muscular de Duchenne, así como afamelanotida —comercializado como Scenesse por la farmacéutica Clinuvel— para tratar la porfiria eritropoyética, una enfermedad genética y poco frecuente que provoca la intolerancia a la luz.
Asimismo, em 2014 también vio la luz la primera recomendación en todo el mundo de una terapia basada en células madre. Se trata de un tratamiento para la insuficiencia límbica (SIL), una afección ocular poco común que puede causar ceguera.
Otras aprobaciones
Sin embargo, el año pasado también fue un buen año para otro tipo de aprobaciones.
En cuanto a medicamentos no huérfanos, la EMA_obtuvo la segunda mejor cifra de los últimos cinco años,superada solamente por los 46 en 2013.
En esta línea, destaca la aprobación de ocho nuevos medicamentos centrados en el área terapéutica de Oncología._Algunos de ellos están dirigidos a carcinomas poco frecuentes y que son, por tanto, difíciles de tratar.
Cabe destacar que para la hepatitis C también se aprobaron novedades terapéuticas, después de haber obtenido todas ellas una evaluación acelerada por parte de las autoridades.
En relación con los medicamentos genéricos, el ritmo se mantiene respecto a los últimos años, aunque la cifra se aleja bastante de las registradas por la agencia hace una década, donde las aprobaciones llegaron a alcanzar el medio centenar por año. No obstante, estos fármacos pueden ser aprobados por la vía descentralizada.